通過相位調制增強3D化學成像
3D 成像極大地幫助了理解復雜的生物和生物醫學系統,它提供了比傳統二維方法更詳細的信息。然而,由于成像速度有限和渾濁環境中的顯著散射等因素,活細胞和組織成像仍然具有挑戰性。
在這種情況下,多模態顯微鏡技術值得注意。具體來說,CRS(相干拉曼散射)等非線性技術使用光學振動光譜,以無標記的方式提供組織和細胞中的精確化學成像。此外,受激拉曼散射(SRS)顯微鏡(一種CRS方法)由于受激拉曼強度與目標分子濃度之間的線性關系,可以準確捕獲生物分子的圖像。它具有高靈敏度,并且不受不需要的非共振背景的干擾。
在最近 發表在 《Advanced Photonics》上的一項研究中,新加坡國立大學設計與工程學院生物醫學工程系光學生物成像實驗室主任黃志偉教授與他的團隊合作開發了一種稱為相位-調制受激拉曼散射斷層掃描 (PM-SRST),用于細胞和組織的無標記 3D 化學成像。
Huang 表示:“我們開發的這種方法可以直接獲取空間域的 3D 樣本信息,無需進行后處理程序。我們還展示了 PM-SRST 技術在提高生物組織 SRS 3D 成像的橫向分辨率和成像深度方面的實用性。”
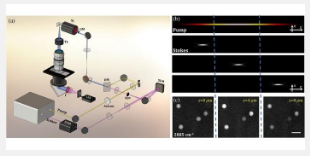
在這種方法中,SRS 方法中的常規“泵浦”光束被稱為貝塞爾光束的專用光束取代。另一束光束(聚焦斯托克斯光束)的位置由稱為空間光調制器的裝置控制,沿著樣品中的貝塞爾泵浦光束,進行機械無掃描 z 切片。此外,通過將貝塞爾泵浦光束與更長波長的斯托克斯光束相結合,PM-SRST 處理散射的能力得到提高,從而可以在更深的組織區域捕獲快速且詳細的圖像。
該方法的有效性通過實驗證明了對不同樣品的快速無標記體積化學成像。其中包括實時監測水中聚合物珠的 3D 布朗運動、觀察植物根部氧化氘 (D 2 O) 的擴散和吸收過程,以及研究乳腺癌細胞對乙酸的生化反應。此外,將 PM-SRST 的光穿透深度與傳統 SRS 成像的光穿透深度進行了比較。在 PM-SRST 中,來自較深組織區域的信號明顯強于 C-SRS,導致成像深度大約提高兩倍。
Huang 指出:“PM-SRST 中的無 z 掃描光學切片特性是通用的,可以輕松擴展到其他成像模式。例如,當前系統可以很容易地適應相干反斯托克斯拉曼散射(CARS)斷層掃描,并且通過單獨利用泵浦或斯托克斯光束,可以簡化PM-SRST技術以促進二次或三次諧波生成斷層掃描,多光子斷層掃描,或熒光斷層掃描。”
PM-SRST 技術能夠進行快速、無標記的 3D 化學成像,可用于研究活細胞和組織內與藥物輸送和治療相關的代謝活動和功能動態過程。
免責聲明:本答案或內容為用戶上傳,不代表本網觀點。其原創性以及文中陳述文字和內容未經本站證實,對本文以及其中全部或者部分內容、文字的真實性、完整性、及時性本站不作任何保證或承諾,請讀者僅作參考,并請自行核實相關內容。 如遇侵權請及時聯系本站刪除。
