YAP/TAZ相互作用可導致對抗腫瘤藥物indisulam產生耐藥性
在健康人體中,組織生長和發育由多種不同的機制協調。在我們的身體內,這些機制調節細胞的健康生長,限制其大小和數量,并通過細胞凋亡控制細胞亡的時間。然而,當這些調節途徑發生改變或破壞時,細胞生長和增殖可能會超過安全范圍,從而導致癌癥。一種關鍵的細胞生長調節機制是Hippo 信號通路。該通路通過轉錄輔激活因子 YAP/TAZ 調節控制細胞增殖和凋亡的幾種基因的表達。這種通路的失調常見于幾種不同的癌癥,包括頭頸部鱗狀細胞癌 (HNSCC)。
一種有前途的抗腫瘤藥物是 indisulam,它是一種細胞周期抑制劑,可抑制細胞增殖基因的表達,并通過降解導致細胞亡的 RNA 結合蛋白 (RBM39) 來觸發異常的 mRNA 剪接。它在細胞培養和動物研究中都表現出了良好的前景。然而,臨床試驗顯示的結果并不那么明確。廣島大學醫院的科學家一直在研究這種對 indisulam 產生耐藥性的原因。廣島大學醫院口腔臨床檢查中心高級講師Toshinori Ando表示: “indisulam 的 臨床試驗
未能顯示出對實體癌患者的良好反應,但耐藥機制尚未解決。我想知道 YAP/RBM39 相互作用是否可能與 indisulam 的耐藥機制有關。” 事實上,他們發現“YAP 與 RBM39 相互作用并產生對 indisulam 的耐藥性,這是未來 indisulam 臨床使用需要解決的關鍵障礙,”Ando 說道。他們的研究結果于 7 月 15 日發表在 《Oncogenesis》雜志上。 信號通路是一系列由信號(通常是環境信號)激活的化學反應。一旦開始,通路內的每個反應都會被依次激活,最終導致特定細胞功能的激活或失活。這使得身體能夠根據細胞當時的需要激活或停用某些基因的轉錄,對特定化學物質(如激素)的存在或缺失做出反應。Hippo 信號通路是一種關鍵通路,它可以通過抑制 YAP/TAZ 來停用控制細胞增殖的基因的轉錄。
抗腫瘤藥物 indisulam 通過降解 RBM39 發揮作用,RBM39 是一種與轉錄因子結合的蛋白質,可增強轉錄并調節基因轉錄過程中不可或缺的 mRNA 剪接。通過降解 RBM39,indisulam 會干擾 RBM39 的正常功能,導致剪接發生變化,從而導致細胞亡,從而減少可能導致腫瘤形成的細胞增殖。
廣島大學的研究人員專注于 YAP/TAZ 轉錄輔激活因子和 RBM39 在細胞核內的反應,以了解它們之間究竟發生了什么。他們還調查了添加 indisulam 后會發生什么,以確定是什么導致了對抗腫瘤藥物的耐藥性。
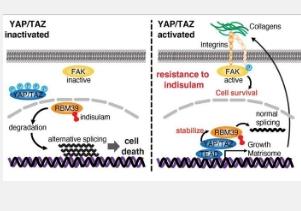
通過蛋白質組分析,該小組確定了 RBM39 與 YAP/TAZ 的相互作用。他們還發現證據表明它確實促進了 YAP/TAZ 的轉錄活性。加入 indisulam 后,它會使粘著斑激酶 (F) 失活,這種酶對于細胞存活非常重要,會導致 RBM39 降解,從而關閉細胞增殖基因的轉錄。
有趣的是,他們發現 indisulam 耐藥性的根源是 YAP/TAZ 的激活。激活后,它會延遲 indisulam 誘導 RBM39 降解的能力,并重新激活 F,從而降低藥物的有效性。YAP/TAZ 的激活在小鼠體內、細胞培養和體外均產生了耐藥性。
“在這項研究中,我們將 RBM39 確定為細胞核中一種新的 YAP/TAZ 相互作用物。值得注意的是,我們證明了 YAP/TAZ 與 RBM39 相互作用,從而產生了對 indisulam 的耐藥性。我們的研究結果揭示了 indisulam 的耐藥機制,這可能有助于開發一種新的治療方法,用于治療包括 HNSCC 在內的實體癌患者,”Ando 說道。
安藤表示,接下來,他們的研究將集中于“進一步研究 RBM39 和 YAP 之間相互作用的機制,從而開發針對該相互作用的新藥,用于治療 HNSCC 等實體癌患者”。
其他貢獻者包括廣島大學醫院口腔臨床檢查中心的片岡奈奈子、新谷智明和梶谷干人; 廣島大學生物醫學與健康科學研究生院口腔腫瘤學系的岡本健人、 上田夢美和矢本壯一;以及 廣島大學生物醫學與健康科學研究生院口腔頜面病理生物學系的
宮內睦。 這項工作得到了 JSPS JP20K18477、JP22H03275 和 JP24K025、廣島大學基金會的“Nozomi h 基金會”以及 JST HIRU-Global 計劃的支持。
免責聲明:本答案或內容為用戶上傳,不代表本網觀點。其原創性以及文中陳述文字和內容未經本站證實,對本文以及其中全部或者部分內容、文字的真實性、完整性、及時性本站不作任何保證或承諾,請讀者僅作參考,并請自行核實相關內容。 如遇侵權請及時聯系本站刪除。
