分子切割和縫合過程可以加速藥物設計
鄧迪大學科學家發明了一種創新的分子“切割和縫合”工藝,可以設計出一種研究工具,加速針對癌癥等沒有其他治療方案的疾病的藥物設計。
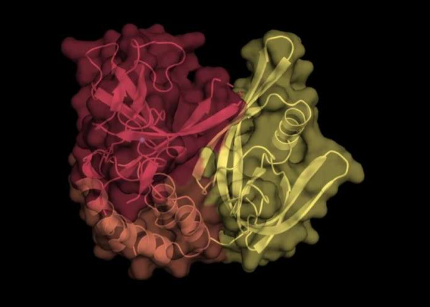
該大學靶向蛋白質降解中心的專家定制了一種蛋白質的新版本,這種蛋白質通常被稱為“蛋白質降解劑”。該過程在將剩余部分縫合在一起之前去除蛋白質中不需要的部分,使研究人員能夠分離蛋白質并在實驗室中更有效地對其進行研究。
這項開創性的研究已發表在《自然通訊》雜志上。
蛋白質降解劑預示著藥物研發領域的一場革命,目前有 50 多種此類藥物正在臨床試驗中接受測試。這類分子的作用方式與傳統藥物的作用方式有著根本的不同。
降解藥物不僅僅阻斷致病蛋白質,還會招募或劫持這些蛋白質,使它們粘附在一種名為泛素 E3 連接酶的重要蛋白質上,該蛋白質是細胞蛋白質回收機制的一部分。這種招募是藥物發揮作用的基礎,可導致致病蛋白質被破壞并從細胞內徹底清除。
目前患者服用的大多數藥物都以這種方式發揮作用,劫持了一種名為 Cereblon (CRBN) 的 E3 連接酶。到目前為止,設計更安全、更像藥物的分子并了解它們如何將致病蛋白招募到 CRBN 的方法一直很緩慢且效率低下。
然而,由結構生物學家 Alena Kroupova 博士和 David Zollman 博士領導的鄧迪團隊在 Alessio Ciulli 教授的指導下,設計出了一種巧妙的方法來設計一種新的蛋白質變體,他們稱之為“CRBN-midi”。
這包括去除蛋白質中不需要的部分,并將剩余部分縫合在一起。這提高了分離蛋白質并在實驗室中對其進行研究的能力。
免責聲明:本答案或內容為用戶上傳,不代表本網觀點。其原創性以及文中陳述文字和內容未經本站證實,對本文以及其中全部或者部分內容、文字的真實性、完整性、及時性本站不作任何保證或承諾,請讀者僅作參考,并請自行核實相關內容。 如遇侵權請及時聯系本站刪除。
